Poniżej przekazuję Państwu treść oficjalnej charakterystyki szczepionki Pfizer BioNTech COVID-19 – w języku polskim. Tłumaczenie, według dostępnych mi informacji, pochodzi z elektronicznego translatora i zostało poprawione (nie jest to profesjonalne tłumaczenie). Materiał źródłowy: charakterystyka produktu leczniczego w języku angielskim.
Zapraszam do wysłuchania wywiadu z lekarzem medycyny Panią dr Dorotą Sienkiewicz, która odnosi się do informacji przedstawionej w charakterystyce szczepionki. Link: wywiad
Ten produkt leczniczy nie ma pozwolenia na dopuszczenie do obrotu w Wielkiej Brytanii, ale zostało wydane zezwolenie na tymczasowe zaopatrzenie Brytyjskiego Departamentu Zdrowia i Opieki Społecznej oraz Agencji Regulacyjnej ds. Leków i Produktów Opieki Zdrowotnej w zakresie czynnej immunizacji w celu zapobiegania chorobie COVID-19 wywoływanej przez wirusa SARS-CoV-2 u osób w wieku 16 lat i starszych. Podobnie jak w przypadku każdego nowego leku w Wielkiej Brytanii, produkt ten będzie ściśle monitorowany, aby umożliwić szybkią identyfikację nowych informacji dotyczących bezpieczeństwa. Pracownicy służby zdrowia są proszeni o zgłaszanie wszelkich podejrzewanych działania niepożądanych.
Aby dowiedzieć się, jak zgłaszać działania niepożądane, patrz punkt 4.8.
1. NAZWA PRODUKTU LECZNICZEGO COVID-19 mRNA Vaccine BNT162b2 koncentrat do sporządzania roztworu do wstrzykiwań
2. SKŁAD JAKOŚCIOWY I ILOŚCIOWY Jest to fiolka wielodawkowa i przed użyciem należy ją rozcieńczyć. 1 fiolka (0,45 ml) zawiera 5 dawek30 mikrogramów RNA BNT162b2 (osadzonego w nanocząsteczkach lipidowych).
Szczepionka mRNA COVID-19 BNT162b2 jest wysoce oczyszczonym jednoniciowym informacyjnym RNA z czapeczką 5 ‘(mRNA) wytwarzany przez bezkomórkową transkrypcję in vitro z odpowiednich matryc DNA, kodujących białko wirusa (S) SARS-CoV-2.
Substancje pomocnicze o znanym działaniu:
Pełny wykaz substancji pomocniczych, patrz punkt 6.1.
3. POSTAĆ FARMACEUTYCZNA Koncentrat do sporządzania roztworu do wstrzykiwań.
Szczepionka jest zamrożonym roztworem o barwie od białej do białawej.
4. SZCZEGÓŁOWE DANE KLINICZNE
4.1 Wskazania terapeutyczne
Czynna immunizacja w celu zapobiegania COVID-19 wywoływanemu przez wirusa SARS-CoV-2 u osób w wieku 16 lat wiek i starsze.
Stosowanie szczepionki COVID-19 mRNA BNT162b2 powinno być zgodne z oficjalnymi wytycznymi.
4.2 Dawkowanie i sposób podawania
Dawkowanie
Osoby w wieku 16 lat i starsze Szczepionkę mRNA COVID-19 BNT162b2 podaje się domięśniowo po rozcieńczeniu w serii dwie dawki (po 0,3 ml) w odstępie 21 dni (patrz punkt 5.1). Nie ma dostępnych danych dotyczących zamienności szczepionki COVID-19 mRNA BNT162b2 z inne szczepionki COVID-19, aby zakończyć serię szczepień. Osoby, które otrzymały jedną dawkę mRNA COVID-19 Szczepionka BNT162b2 powinna otrzymać drugą dawkę mRNA COVID-19
Szczepionka BNT162b2 uzupełniająca serię szczepień.
Osobnikom można zapewnić ochronę dopiero po co najmniej 7 dniach od podania drugiej dawki szczepionki.
Więcej informacji na temat skuteczności, patrz punkt 5.1.
Populacja pediatryczna Bezpieczeństwo i skuteczność szczepionki COVID-19 mRNA BNT162b2 u dzieci poniżej 16 roku życia nie zostały jeszcze ustalone.
Sposób podawania
Podać szczepionkę COVID-19 mRNA Vaccine BNT162b2 domięśniowo w mięsień naramienny po rozcieńczeniu. Szczepionki nie należy wstrzykiwać donaczyniowo, podskórnie ani śródskórnie.
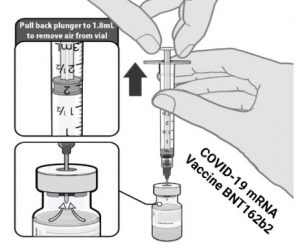
Przygotowanie: Wielodawkową fiolkę przechowuje się w stanie zamrożonym i przed rozcieńczeniem należy ją rozmrozić.
Instrukcja usuwania, patrz punkt 6.6.
4.3 Przeciwwskazania
Nadwrażliwość na substancję czynną lub na którąkolwiek substancję pomocniczą wymienioną w punkcie 6.1.
4.4 Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania Identyfikowalność.
W celu poprawy identyfikowalności biologicznych produktów leczniczych – nazwę i numer serii podawanego produktu należy wyraźnie odnotować.
Ogólne zalecenia
Podobnie jak w przypadku wszystkich szczepionek do wstrzykiwań, zawsze powinno być odpowiednie leczenie i nadzór medyczny łatwo dostępne w przypadku rzadkiego zdarzenia anafilaktycznego po podaniu szczepionki.
Podanie szczepionki COVID-19 mRNA BNT162b2 należy odroczyć u osób cierpiących na ostrą, ciężką chorobę przebiegającą z gorączką.
Osoby otrzymujące terapię przeciwzakrzepową lub osoby z zaburzeniami krzepnięcia, które mogą być przeciwwskazanenie należy podawać szczepionki we wstrzyknięciu domięśniowym, chyba że potencjalne korzyści wyraźnie przeważają ryzyko podania.
Osoby z obniżoną odpornością, w tym osoby otrzymujące leczenie immunosupresyjne, mogą mieć osłabiona odpowiedź immunologiczna na szczepionkę. Brak danych dotyczących jednoczesnego stosowanialeki immunosupresyjne.
Jak w przypadku każdej szczepionki, szczepienie szczepionką COVID-19 mRNA BNT162b2 może nie chronić wszystkich biorców szczepionki.
Brak danych na temat stosowania szczepionki COVID-19 mRNA BNT162b2 u osób które mają wcześniej otrzymali pełną lub częściową serię szczepionek z inną szczepionką COVID-19. Informacje pomocnicze
Ta szczepionka zawiera mniej niż 1 mmol (39 mg) potasu na dawkę, tzn. Zasadniczo „nie zawiera potasu”.
Ta szczepionka zawiera mniej niż 1 mmol sodu (23 mg) na dawkę, tj. Zasadniczo „nie zawiera sodu”.
4.5 Interakcje z innymi produktami leczniczymi i inne formy interakcji
Nie przeprowadzono badań interakcji.
Jednoczesne podanie szczepionki COVID-19 mRNA BNT162b2 z innymi szczepionkami nie zostało zbadane (patrz punkt 5.1).
Nie mieszaj szczepionki COVID-19 mRNA BNT162b2 z innymi szczepionkami / produktami w tej samej strzykawce.
4.6 Płodność, ciąża i laktacja
Ciąża
Brak jest danych dotyczących stosowania szczepionki COVID-19 mRNA BNT162b2 lub są one ograniczone.
Badania toksyczności reprodukcyjnej zwierząt nie zostały zakończone.
Szczepionka COVID-19 mRNA
Nie zaleca się stosowania BNT162b2 w czasie ciąży.
W przypadku kobiet w wieku rozrodczym przed szczepieniem należy wykluczyć ciążę. Ponadto kobiety w wieku rozrodczym należy zalecić unikanie ciąży przez co najmniej 2 miesiące po podaniu drugiej dawki.
Karmienie piersią
Nie wiadomo, czy szczepionka BNT162b2 mRNA COVID-19 przenika do mleka ludzkiego. Ryzykonie można wykluczyć noworodków / niemowląt. Nie należy stosować szczepionki COVID-19 mRNA BNT162b2 podczas karmienia piersią.
Płodność
Nie wiadomo, czy szczepionka BNT162b2 przeciwko COVID-19 mRNA ma wpływ na płodność.
4.7 Wpływ na zdolność prowadzenia pojazdów i obsługiwania maszyn Szczepionka mRNA COVID-19 BNT162b2 nie ma lub ma znikomy wpływ na zdolność prowadzenia pojazdów i używania maszyn. Jednak niektóre z działań niepożądanych wymienionych w punkcie 4.8 mogą przejściowo wpływać na zdolność prowadzenia pojazdów i obsługiwania maszyn.
4.8 Działania niepożądane
Podsumowanie profilu bezpieczeństwa Bezpieczeństwo szczepionki COVID-19 mRNA BNT162b2 oceniono u uczestników w wieku 16 lati starszych w dwóch badaniach klinicznych przeprowadzonych w Stanach Zjednoczonych, Europie, Turcji, Afryce Południowej i Ameryka Południowa. Do badania BNT162-01 (badanie 1) włączono 60 uczestników w wieku od 18 do 55 lat.
W badaniu C4591001 (badanie 2) wzięło udział około 44 000 uczestników w wieku 12 lat lub starszych.
W badaniu 2 łącznie 21,720 uczestników w wieku 16 lat lub starszych otrzymało co najmniej jedną dawkę COVID-19 mRNA Szczepionka BNT162b i 21 728 uczestników w wieku 16 lat lub starszych otrzymało placebo. Na zewnątrz z nich, w czasie analizy, 19067 (9531 COVID-19 mRNA Vaccine BNT162b2 i9536 placebo) oceniano pod kątem bezpieczeństwa 2 miesiące później druga dawka Szczepionki COVID-19 mRNABNT162b2.
Cechy demograficzne były ogólnie podobne pod względem wieku, płci, rasy i pochodzenia etnicznego wśród uczestników, którzy otrzymali szczepionkę COVID-19 mRNA i tych, którzy otrzymali placebo.
Ogółem wśród uczestników, którzy otrzymali szczepionkę COVID-19 mRNA BNT162b2, 51,5%mężczyźni i 48,5% to kobiety, 82,1% było rasy białej, 9,6% było rasy czarnej lub Afroamerykanie, 26,1% było Hiszpanie / Latynosi, 4,3% to Azjaci, a 0,7% to rdzenni Amerykanie / rdzenni mieszkańcy Alaski.
Najczęstszymi działaniami niepożądanymi u uczestników w wieku 16 lat i starszych był ból podczas wstrzyknięcia miejscu (> 80%), zmęczenie (> 60%), ból głowy (> 50%), bóle mięśni (> 30%), dreszcze (> 30%), bóle stawów (> 20%)i gorączka (> 10%), zwykle o łagodnym lub umiarkowanym nasileniu i ustępująca w ciągu kilku dni po szczepieniu. W razie potrzeby leczenie objawowe lekami przeciwbólowymi i / lub przeciwgorączkowymi można stosować produkty (np. produkty zawierające paracetamol).
Działania niepożądane z badań klinicznych
Działania niepożądane zgłaszane w badaniach klinicznych są wymienione w tym punkcie według układów i narządów MedDRA klasa, w kolejności malejącej częstotliwości i powagi. Częstotliwość definiuje się następująco: bardzoczęsto (≥ 1/10), często (≥ 1/100 do <1/10), niezbyt często (≥ 1/1 000 do <1/100), rzadko (≥ 1/10 000 do <1/1 000), bardzo rzadko (<1/10 000), nieznana (częstość nie może być określona na podstawie dostępne dane).
Zaburzenia krwi i układu chłonnego
Niezbyt często: limfadenopatia
Zaburzenia układu nerwowego
Bardzo często: ból głowy
Zaburzenia mięśniowo-szkieletowe i tkanki łącznej
Bardzo często: bóle stawów; mialgia
Zaburzenia ogólne i stany w miejscu podania
Bardzo często: ból w miejscu wstrzyknięcia; zmęczenie; dreszcze; gorączka
Często: zaczerwienienie w miejscu wstrzyknięcia; obrzęk w miejscu wstrzyknięcia
Niezbyt często: złe samopoczucie
Zaburzenia żołądkowo-jelitowe
Często nudności
Zgłaszanie podejrzewanych działań niepożądanych
Zgłaszanie podejrzewanych działań niepożądanych po dopuszczeniu produktu leczniczego do obrotu jest ważne. To umożliwia ciągłe monitorowanie stosunku korzyści do ryzyka produktu leczniczego.
Opieka zdrowotna
Profesjonaliści są proszeni o zgłaszanie wszelkich podejrzewanych działań niepożądanych za pośrednictwem Żółtej Karty Koronawirusa strona zgłaszająca https://coronavirus-yellowcard.mhra.gov.uk/lub poszukaj MHRA Yellow Card w Google Play lub Apple App Store i podać markę szczepionki i numer serii partii, jeśli jest dostępny.
4.9 Przedawkowanie
Uczestnicy, którzy otrzymali 58 mikrogramów szczepionki COVID-19 mRNA w badaniach klinicznych, nie otrzymali zgłosić wzrost reaktogenności lub zdarzeń niepożądanych.
W przypadku przedawkowania należy monitorować czynności życiowe i możliwe leczenie objawowe
Zalecana.
5. WŁAŚCIWOŚCI FARMAKODYNAMICZNE
5.1 Właściwości farmakodynamiczne
Grupa farmakoterapeutyczna: {grupa}, kod ATC: jeszcze nie przydzielony
Mechanizm akcji Modyfikowany nukleozydem informacyjny RNA w szczepionce COVID-19 mRNA BNT162b2 jest sformułowany w nanocząsteczki lipidowe, które umożliwiają dostarczanie RNA do komórek gospodarza, aby umożliwić ekspresję SARS-Antygen S CoV-2. Szczepionka wywołuje zarówno neutralizujące przeciwciała, jak i komórkową odpowiedź immunologiczną nakolec (S) antygen, który może przyczynić się do ochrony przed chorobą COVID-19.
Skuteczność u uczestników w wieku 16 lat i starszych
Skuteczność szczepionki COVID-19 mRNA BNT162b2 oceniano u uczestników w wieku 16 lat i starszych w dwóch badaniach klinicznych przeprowadzonych w Stanach Zjednoczonych, Europie, Turcji, RPA i Ameryka Południowa. Do badania 1 włączono 60 uczestników w wieku od 18 do 55 lat. Badanie 2 to wieloośrodkowe ,badanie skuteczności kontrolowane placebo u uczestników w wieku 12 lat i starszych. Randomizacja była stratyfikowane według wieku: od 12 do 15 lat, od 16 do 55 lat lub od 56 lat i starszych,co najmniej 40% uczestników z warstwy ≥ 56 lat. Z badania wykluczono uczestników, którzy byli z obniżoną odpornością i ci, którzy mieli wcześniej kliniczną lub mikrobiologiczną diagnozę Choroba COVID-19. Uczestnicy z istniejącą wcześniej stabilną chorobą, zdefiniowaną jako choroba niewymagająca istotna zmiana terapii lub hospitalizacji z powodu pogorszenia choroby w ciągu 6 tygodni wcześniej rekrutacji, jak byli uczestnicy ze znaną stabilną infekcją człowieka wirus niedoboru odporności (HIV), wirus zapalenia wątroby typu C (HCV) lub wirus zapalenia wątroby typu B (HBV). Nie było wymóg profilaktycznego stosowania paracetamolu lub leków przeciwbólowych. Mogłyby być szczepionki przeciw grypie podawana poza oknem ± 14 dni dawek szczepionki.
W badaniu 2 około 44 000 uczestnicy w wieku 12 lat i starsi zostali zrandomizowani jednakowo i otrzymali 2 dawki Szczepionki COVID-19 mRNA lub placebo w planowanym odstępie 21 dni. Plikanalizy skuteczności obejmowały uczestników, którzy otrzymali drugą szczepionkę w ciągu 19 do 42 dnipo ich pierwszym szczepieniu. Planowany czas obserwacji uczestników to 24 miesiąceoceny bezpieczeństwa i skuteczności przeciwko chorobie COVID-19.
Populacja do analizy pierwszorzędowego punktu końcowego skuteczności obejmowała 36 621 uczestników 12 latw wieku i starszych (18242 w grupie szczepionki COVID-19 mRNA i 18379 w grupie placebo)którzy nie mieli dowodów wcześniejszego zakażenia SARS-CoV-2 do 7 dni po drugiej dawce.
Cechy demograficzne były ogólnie podobne pod względem wieku, płci, rasy i pochodzenia etnicznego wśród uczestników, którzy otrzymali szczepionkę COVID-19 mRNA BNT162b2 i tych, którzy ją otrzymali placebo. Ogólnie wśród uczestników, którzy otrzymali szczepionkę COVID-19 mRNA, 51,1% stanowili mężczyźnia 48,9% stanowiły kobiety, 82,8% było rasy białej, 8,9% było rasy czarnej lub Afroamerykanów, 26,8%Hiszpanie / Latynosi, 4,5% to Azjaci, a 0,6% to rdzenni Amerykanie / rdzenni mieszkańcy Alaski. 57,2% było w wieku 16-55 lat, 42,6% było w wieku> 55 lat, a 21,8% było w wieku ≥ 65 lat.
Skuteczność przeciwko chorobie COVID-19
W momencie analizy badania 2 przedstawione informacje opierają się na uczestnikach w wieku 16 lat i starszy. Uczestnicy byli obserwowani pod kątem objawowej choroby COVID-19 przez co najmniej 2214 osobo lat w przypadku szczepionki COVID-19 mRNA i co najmniej 2222 osobo lat w grupie placebo.
W grupie szczepionki COVID-19 mRNA zidentyfikowano 8 potwierdzonych przypadków COVID-19 i 162 odpowiednio w grupie placebo. W tej analizie, w porównaniu z placebo, skuteczność COVID-19
Szczepionka mRNA BNT162b2 z pierwsze wystąpienie COVID-19 u uczestników od 7 dni po 2 dawcebez dowodów wcześniejszego zakażenia SARS-CoV-2 wyniósł 95,0% (95% wiarygodny przedział 90,3% do97,6%). U uczestników w wieku 65 lat i starszych oraz w wieku 75 lat i starszych bez dowodów wcześniejsze zakażenia SARS-CoV-2, skuteczność szczepionki COVID-19 mRNA BNT162b2 wyniosła 94,7%(dwustronny 95% przedział ufności od 66,7% do 99,9%) i 100% (dwustronny 95% przedział ufności przedział od -13,1% do 100,0%).
W oddzielnej analizie, w porównaniu z placebo, skuteczność szczepionki COVID-19 mRNA od początku Wystąpienie COVID-19 od 7 dni po dawce 2 u uczestników z wcześniejszymi dowodami lub bez zakażenie SARS-CoV-2 wyniosło 94,6% (95% wiarygodny przedział od 89,9% do 97,3%).
Nie było znaczących różnic klinicznych w ogólnej skuteczności szczepionki u uczestników, którzy byli na ryzyko ciężkiej choroby COVID-19, w tym osób z co najmniej jedną chorobą współistniejącą, która zwiększa ryzyko ciężkiej choroby COVID-19 (np. astma, BMI ≥ 30 kg / m2, przewlekła choroba płuc, cukrzyca mellitus, nadciśnienie).
Potwierdzone przypadki określono metodą reakcji łańcuchowej polimerazy z odwrotną transkrypcją (RT-PCR)i co najmniej 1 objaw zgodny z chorobą COVID-19 *.
* Definicja przypadku (co najmniej 1 z): gorączka, nowy lub nasilony kaszel, nowa lub zwiększona duszność; dreszcze, nowy lub zwiększony ból mięśni, nowy utrata smaku lub węchu, ból gardła, biegunka lub wymioty.
5.2 Właściwości farmakokinetyczne
Nie dotyczy.
5.3 Przedkliniczne dane o bezpieczeństwie
Dane niekliniczne wynikające z konwencjonalnego badania dawki wielokrotnej nie ujawniają żadnego szczególnego zagrożenia dla człowieka toksyczność. Nie przeprowadzono badań na zwierzętach dotyczących potencjalnego toksycznego wpływu na reprodukcję i rozwój zakończony.
6. DANE FARMACEUTYCZNE
6.1 Wykaz substancji pomocniczych
ALC-0315 = (4-hydroksybutylo) azanodiylo) bis (heksano-6,1-diylo) bis (2-heksylodekanian),ALC-0159 = 2 – [(glikol polietylenowy) -2000] -N, N-ditetradecyloacetamid, 1,2-distearoilo-sn-glicero-3-fosfocholina, cholesterol,chlorek potasu, dwuwodorofosforan potasu,chlorek sodu,dwuwodny wodorofosforan disodu,sacharoza,woda do wstrzykiwań
6.2 Niezgodności farmaceutyczne
Ze względu na brak badań zgodności, tego produktu leczniczego nie wolno mieszać z innymi lekamiprodukty.
6.3 Okres trwałości
6 miesięcy w temperaturze od -80 ° C do -60 ° C.
6.4 Specjalne środki ostrożności podczas przechowywania
Przechowywać w zamrażarce w temperaturze od -80 ° C do -60 ° C.
Przechowywać w pojemniku termicznym w temperaturze od -90 ºC do -60 ºC.
Przechowywać w oryginalnym opakowaniu w celu ochrony przed światłem.
Po rozmrożeniu szczepionkę należy rozcieńczyć i natychmiast zużyć. Jednak dane dotyczące stabilności podczas użytkowania wykazali, że po rozmrożeniu nierozcieńczoną szczepionkę można przechowywać do 5 dni w temperaturze od 2 ° C do8 ° C lub do 2 godzin w temperaturze do 25 ° C przed użyciem.
Podczas przechowywania minimalizować narażenie na światło w pomieszczeniu i unikać bezpośredniego nasłonecznienia i światła ultrafioletowego. Rozmrożonymi fiolkami można manipulować warunki oświetlenia w pomieszczeniu.
Po rozcieńczeniu szczepionkę przechowywać w temperaturze od 2 ° C do 25 ° C i zużyć natychmiast w ciągu 6 godzin. Szczepionka nie zawiera konserwantów. Wyrzucić niewykorzystaną szczepionkę.
Po rozcieńczeniu fiolki należy oznaczyć nową datą i godziną wyrzucenia. Po rozmrożeniu plikszczepionki nie można ponownie zamrażać.
6.5 Rodzaj i zawartość opakowania Koncentrat do sporządzania roztworu dla 5 dawek w przezroczystej fiolce (szkło typu I) o pojemności 2 ml z korkiem(bromobutyl) i zdejmowaną plastikową nasadkę z aluminiową uszczelką.Wielkość opakowania: 195 fiolek.
6.6 Specjalne środki ostrożności dotyczące usuwania i innego postępowania
Wszelkie niewykorzystane resztki produktu leczniczego lub jego odpady należy usunąć zgodnie z lokalnymi przepisami wymagania.
Instrukcja dotycząca przygotowania dawki produktu leczniczego przed podaniem, patrz punkt 4.2.
7. PODMIOT ODPOWIEDZIALNY PODMIOT ODPOWIEDZIALNY
Nie dotyczy.
8. NUMER POZWOLENIA NA DOPUSZCZENIE DO OBROTU
Nie dotyczy.
9. DATA WYDANIA PIERWSZEGO POZWOLENIA NA DOPUSZCZENIE DO OBROTU / DATA PRZEDŁUŻENIA POZWOLENIA
Nie dotyczy .

Posiadając dostęp do internetowej bazy wiedzy ZE ŹRÓDEŁ możemy sprawdzić sami, na kim BIGFarma ma zamiar robić interesy. I nie tylko to możemy zweryfikować sami.
Definicja wirusa powstała 60 lat temu. Nie ma żadnej naukowej wartości. Nigdy nie została naukowo zweryfikowana. O koncepcji filozoficznej powstania definicji nukleoproteiny czyli wirusa, wypowiedział się jej twórca w swoim wykładzie noblowskim https://www.nobelprize.org/prizes/medicine/1965/lwoff/biographical/
Medycyna współczesna bazuje na XIX wiecznej teorii infekcyjności – nigdy naukowo nie potwierdzonej – koncepcji konfabulanta Ludwika Pasteura i Roberta Kocha (życiorys L Pasteura na podstawie osobistych notatek naukowca napisał Gerald Geison)
Na teorii infekcyjności bazuje bigfarma tworząc bezwartościowe, szkodliwe produkty, rzekomo biologicznie aktywne, teoretycznie “wywołujące odporność”. Praktycznie – trucizny, które organizm musi unieszkodliwiać ze względu na ich skład.
Proces technologiczny produkcji szczepionek jest w sieci -https://bladymamut.files.wordpress.com/2015/03/technologie-wytwarzania-szczepionek.pdf
Prawie 50 lat temu powstał nowy paradygmat medyczny. Oparty na ontologii, embriologii, histologii, naukach biologicznych. Czyli ścisłych. Niedopuszczony do ujawnienia. Historia lekarza, któremu dane było odkryć BIOLOGICZNE REAKCJE ssaków do których należy człowiek jest zawarta w https://pl.germanischeheilkunde-drhamer.com/
Film 5 Praw Natury
https://www.youtube.com/watch?v=d-nS_vEOliA